Материалы конгрессов и конференций
VII РОССИЙСКАЯ ОНКОЛОГИЧЕСКАЯ КОНФЕРЕНЦИЯ
ТЕХНИКА И НЕПОСРЕДСТВЕННЫЕ РЕЗУЛЬТАТЫ ОПЕРАЦИЙ ПО ПОВОДУ РАКА ПРЯМОЙ КИШКИ, СОПРОВОЖДАЮЩИХСЯ СОХРАНЕНИЕМ ВЕГЕТАТИВНОЙ НЕРВНОЙ СИСТЕМЫ ОРГАНОВ МАЛОГО ТАЗА
Г.И. Воробьев, Т.С. Одарюк, Л.Л. Капуллер, П.В. Царьков, В.Н. Кашников, А.А. Троицкий, Д.Ю. Пикунов
ГНЦ Колопроктологии МЗ РФ, Москва
Операции, сопровождающиеся сохранением вегетативной нервной системы (ВНС) органов полости малого таза, являются сравнительно молодым направлением в абдоминальной хирургии. Наибольшее распространение они получили при выполнении различных типов резекций прямой кишки при ее неопластическом поражении, что в первую очередь связано с близостью расположения анатомических структур ВНС и границ резекции кишки. Тем самым, развитие техники нервосохраняющих операций напрямую связано с развитием хирургии рака прямой кишки.
Так в 80-х годах, основным принципом хирургии рака прямой кишки было максимальное удаление клетчатки из полости малого таза. При этом граница резекции определялась хирургом самостоятельно в меру своего представления об анатомии малого таза и предшествующего хирургического опыта. При этом оставление части клетчатки увеличивало риск возникновения возврата заболевания, а необоснованно «избыточный радикализм» приводил к увеличению частоты мочеполовых расстройств.
Именно в этот период получает максимальное развитие проведение пред- и/или послеоперационной лучевой терапии (ЛТ) как метода, направленного на снижение частоты местного возврата заболевания.
С 90-х годов в анатомии прямой кишки появляется такое понятие как «мезоректум», в которое входит совокупность тканей, располагающихся между стенкой прямой кишки и ее висцеральной фасцией, а в хирургии рака прямой кишки – «мезоректумэктомия». Таким образом, были четко определены границы удаления клетчатки полости малого таза при выполнении стандартных оперативных вмешательств. Использование только данного приема позволило снизить частоту развития местных рецидивов до 10%.
Проведенные в последние два десятилетия исследования, направленные на изучение эффективности лучевого воздействия, сравнивающие онкологическую эффективность операций, сопровождавшихся тотальной мезоректумэктомией по сравнению с пред- и/или послеоперационной ЛТ, не выявили статистически значимого улучшения показателей частоты местного возврата заболевания и 5-летней выживаемости.
Таким образом, хирургическое лечение рака прямой кишки вновь подтвердило свое превалирующее значение. Именно в этот период получили свое развитие операции, сопровождающиеся сохранением ВНС и названные нервосохраняющей хирургией (НСХ).
Исторически вмешательства с сохранением ВНС начали применяться при операциях, сопровождающихся выполнением расширенной аорто-подвздошно-тазовой лимфаденэктомией (АПТ ЛАЭ). Это связано с тем, что при выполнении операций, дополненных лимфодиссекцией, уровень урологических расстройств гораздо выше, чем при операциях без нее. Это и определило дальнейшее развитие хирургии рака прямой кишки в сторону сочетания стандартной техники с полным или частичным сохранением ВНС. Полученные результаты показали снижение уровня мочевыделительных расстройств после НСХ.
С другой стороны, сохранение вегетативных нервных структур таза в силу их анатомического расположения напрямую связано с сохранением целостности висцеральной фасции прямой кишки, что является ключевым требованием для правильного выполнения тотальной мезоректумэктомии, что в свою очередь связано с улучшением отдаленных (онкологических) результатов. Именно это обстоятельство в последнее время способствует увеличению интереса к данного рода операциям.
Вначале необходимо остановиться на некоторых анатомических и физиологических аспектах ВНС, тем более что до настоящего времени в литературе мы не встретили единой номенклатурной терминологии различных анатомических образований ВНС.
ВНС таза представлена симпатической и парасимпатической частями. Симпатическая часть берет начало от вентральных корешков Th12-L3 сегментов спинного мозга. При выходе из позвоночных отверстий они идут общим пучком, называемым поясничным висцеральным нервом (n. splanchnicus lumbalis). На уровне тела L5 позвонка нерв соединяется на передней поверхности аорты с таким же пучком противоположной стороны, образуя верхнее гипогастральное сплетение (pl. hypogastricus sup.). Верхнее гипогастральное сплетение представляет собой лентовидный тяж шириной около 5 мм и длиной около 40 мм, формирующийся на уровне бифуркации аорты. На уровне межпозвоночного диска L5-S1 данное сплетение разделяется на правый и левый гипогастральные нервы (nn. hypogastricus dexter et sinister). Спускаясь в полость малого таза, указанные нервы идут в латеральном направлении, достигая тазового сплетения (pl. pelvici) на боковой стенке таза. Парасимпатическая часть ВНС таза начинается из вентральных корешков S3-S4 сегментов спинного мозга у мужчин и S2-S4 у женщин. Они входят в полость таза через крестцовые отверстия. Далее крестцовые вегетативные нервы (nn. sacralis) спускаются вниз по боковой стенке до тазового сплетения. Тазовое сплетение представляет собой переплетение симпатических и парасимпатических волокон. Это ромбовидной формы чешуевидное образование нервной ткани размером около 3х4 см и толщиной около 1 мм, располагающееся на боковой стенке таза. Тазовое сплетение лежит в толще поверхностного листка париетальной фасции и отдает ветви к урогенитальным органам таза и прямой кишке.
Парасимпатические нервы отвечают за увеличение притока крови к половому члену, обуславливающее эрекцию, а также к влагалищу и наружным половым органам у женщин, обуславливающее набухание половых губ и клитора. Парасимпатическая часть нервной системы таза стимулирует также сокращение m. detrusor, что ведет к осуществлению нормального акта мочеиспускания. Симпатические нервы отвечают за семяизвержение и ритмические сокращения половых путей в течение оргазма у мужчин и, возможно, у женщин. Симпатические нервы также ингибируют сокращение детрузора и вызывают констрикцию шейки мочевого пузыря, регулируя его функцию. Проприоцептивные афферентные волокна от рецепторов в стенке мочевого пузыря, отвечающие за ощущение полноты пузыря, идут по такому же пути, как и парасимпатические нервы.
Выполнение нервосохраняющих операций подразумевает под собой полное или частичное сохранение ВНС. В зависимости от степени сохранения нервных образований разные авторы предлагают свои классификации подобных вмешательств. Наиболее полной и удобной является классификация, предложенная N. Saito. Он подразделяет проводимые операции на 6 типов:
Техника нервосохраняющей хирургии. Как уже было отмечено, НСХ – это операции, сопровождающиеся полным либо частичным сохранением ВНС органов малого таза. Наиболее часто повреждение ВНС наблюдаются при выполнении тотальной мезоректэктомии. С целью предупреждения травматизации нервных стволов и сплетений при выполнении операций необходимо акцентировать внимание на следующих этапах мобилизации прямой кишки.
Во-первых, при перевязке нижней брыжеечной артерии у места ее отхождения от аорты возможно повреждение нижнебрыжеечного сплетения, а также поясничных внутренностных нервов, особенно левого. Для предотвращения этого после выделения артерии необходимо «скелетизировать» начальный ее отрезок, подготовив место для перевязки. Следует также визуализировать поясничные внутренностные нервы, лежащие по бокам от аорты и избежать их травматизации.
Во-вторых, при выделении задней стенки прямой кишки на уровне промонториума возможно повреждение гипогастральных нервов. Во избежание этого мобилизацию следует проводить строго по задней поверхности мезоректальной фасции. Ключом к выбору правильного направления может служить расположение верхней прямокишечной артерии: она лежит сразу же кпереди от мезоректальной фасции на уровне промонториума. При этом гипогастральные нервы находятся под постоянным визуальным контролем на протяжении от верхнего гипогастрального сплетения до соединения с тазовым сплетением.
Третьим моментом, на который следует обратить внимание, является идентификация и мобилизация боковой стенки прямой кишки в области средней прямокишечной артерии и тазового сплетения. Для избежания травмы тазового сплетения необходимо четко придерживаться хода висцеральной фасции в области боковой стенки, избегая сильных тракций кишки. Пересекать многочисленные нейро-васкулярные пучки, проходящие через межфасциальное пространство, следует острым путем или электрокаутером при активной кровоточивости. При наличии четко выраженной средней прямокишечной артерии кровотечение из-за ее пересечения редко бывает значительным вследствие ее малого размера.
В случае, когда необходимо выполнение расширенной АПТ ЛАЭ, указанные нервные структуры отделяются от подлежащей париетальной фасции таза. Особенно следует быть осторожными при выделении сакральных нервов, вследствие их плотного сращения с последней.
В Государственном Научном Центре Колопроктологии с 1999 по 2003 гг. в рамках проспективного рандомизированного исследования по изучению эффективности расширенных операций с АПТ ЛАЭ накоплен опыт выполнения 21 оперативного вмешательства с различными модификациями НСХ. В указанную группу вошли 10 мужчин и 11 женщин. Средний возраст составил 52,2 (39-74) года. Распределение пациентов по уровню сохранения элементов ВНС представлено в табл. 1.
Таблица 1.
Распределение пациентов по уровню сохранения элементов ВНС.
| Уровень сохранения элементов ВНС | Число больных |
|---|---|
| Полное сохранение ВНС | 10 |
| Одностороннее сохранение ВНС (удален гипогастральный нерв и тазовое сплетение с одной стороны) | 5 |
| Одностороннее сохранение гипогастрального нерва | 4 |
| Одностороннее сохранение тазового сплетения | 1 |
| Одностороннее сохранение S3-S4 крестцовых нервов | 1 |
Кроме того, 9 пациентам в ходе АПТ ЛАЭ элементы ВНС таза были удалены полностью. Из них 2 мужчин и 7 женщин, средний возраст составил 54,3 (29–68) года.
В послеоперационном периоде была оценена частота возникновения мочевых расстройств в зависимости от уровня сохранения ВНС (табл. 2).
После операций, сопровождавшихся полным удалением вегетативной иннервации органов таза, самостоятельное мочеиспускание восстановлено у всех 9 пациентов. Однако у 2 из них в послеоперационном периоде наблюдались явления стойкой атонии мочевого пузыря, что при неэффективности консервативной терапии в течение 15 дней послужило поводом к постановке эпицистостомического катетера. В дальнейшем самостоятельное мочеиспускание восстановилось. У 4 (44%) пациентов в раннем послеоперационном периоде развилась рефлекторная задержка мочеиспускания, явления которой были купированы консервативно. Стоит отметить, что во всех наблюдениях отсутствовали прежние позывы на мочеиспускание.
У всех больных после выполнения операции с полным сохранением ВНС было восстановлено самостоятельное мочеиспускание в сроки от 2 до 4 дней после оперативного вмешательства, то есть сразу после первого удаления трансуретрального катетера. При этом все 10 пациентов отмечали сохранение прежних позывов на мочеиспускание.
После операций, сопровождавшихся односторонним удалением элементов ВНС таза, у одной из 11 больных развилась атония мочевого пузыря. После проведения медикаментозной и электростимуляции на 15 сутки самостоятельное мочеиспускание у нее было восстановлено. Прежние позывы на мочеиспускание сохранены у 4 пациентов.
Таблица 2. Частота развития мочевых расстройств в зависимости от уровня сохранения ВНС.
| Стойкая атония мочевого пузыря (n) | Рефлекторная задержка мочеиспускания (n) | Сохранение позывов на мочеиспускание (n) | |
|---|---|---|---|
| ВНС таза удалена (n=9) | 2 | 4 | 0 |
| Полное сохранение ВНС таза (n=10) | 0 | 0 | 10 |
| Одностороннее сохранение ВНС (удален гипогастральный нерв и тазовое сплетение с одной стороны) (n=5) | 1 | 1 | 4 |
| Одностороннее сохранение гипогастрального нерва (n=4) | 4 | 0 | 1 |
| Одностороннее сохранение тазового сплетения (n=1) | 0 | 0 | 1 |
| Одностороннее удаление S3-S4 крестцовых нервов (n=1) | 0 | 0 | 1 |
Анализируя полученные результаты, хотелось бы отметить тот факт, что значительная часть операций, сопровождавшихся полным удалением ВНС таза или отдельных ее частей, произведена в начальные периоды нашей работы. Это связано с моментами отработки техники операции, накопления опыта. В последнее время мы стараемся максимально щадяще относиться к элементам вегетативной иннервации.
Таким образом, использование техники сохранения ВНС таза даёт возможность снижения уровня мочеполовых расстройств при операциях по поводу рака прямой кишки, причем максимально полное сохранение элементов ВНС таза ведет к лучшим функциональным результатам. Кроме того, использование НСХ при стандартных операциях позволяет выполнять тотальную мезоректумэктомию без повреждения висцеральной фасции, что на сегодняшний день является наиболее важным фактором, позволяющим существенно уменьшить число местных рецидивов заболевания. Именно поэтому овладение нервосохраняющей техникой должно стать необходимым элементом в арсенале хирургов, занимающихся лечение рака прямой кишки.
Особенности внутрикишечной опухолевой инвазии в проксимальном направлении при раке прямой кишки
И.А. Нечай, Г.И. Суханкина
Городская больница № 40
СПбГУ, медицинский факультет, кафедра хирургии
Аннотация. Представлены результаты гистологических исследований распространения «ракового поля» в проксимальном направлении при раке прямой кишки. Необходимость таких исследований обусловлена важностью сохранения дистальных отделов сигмовидной кишки, при выполнении передней резекции прямой кишки, с целью улучшения резервуарной и эвакуаторной функций. В результате определено минимальное расстояние от верхнего края опухоли, которое необходимо отступить при пересечении кишки, не нарушая онкологических принципов оперирования.
Клинические наблюдения о несомненной важности бережного отношения к дистальной части сигмовидной кишки при передних резекциях прямой кишки (ПК), побудили нас изучить распространенность ракового поля в проксимальном направлении от верхнего края раковой опухоли. Знания эти должны лечь в основу рекомендаций, насколько минимально допустимо отступать от верхнего края опухоли при резекции сигмовидной кишки, не нарушая онкологических принципов оперирования. Такая озабоченность связана с тем, что у больных, у которых при резекции ПК для анастомоза использовалась самая дистальная часть низводимой сигмовидной кишки, резервуарно-накопительная и эвакуаторная функции оказывались заметно лучше. Вместе с тем, заботясь об улучшении функциональных результатов операций, мы постоянно имели в виду важность соблюдения онкологических принципов оперирования, поскольку главным при лечении онкологических больных является, конечно, улучшение пятилетней выживаемости.
Распространение ракового процесса внутристеночно от края видимой опухоли ПК в дистальном направлении привлекало внимание ряда авторов. Такие исследования имеют чрезвычайно важное значение при оперативном лечении больных с низкой раковой опухолью ПК. При этой локализации злокачественной опухоли, с позиций функциональных результатов, важен каждый сантиметр сохраненной дистальной части кишки. Использование сшивающих аппаратов при резекции ПК позволяет в техническом плане проводить максимально низкие резекции кишки.
Распространенность инвазии в дистальном направлении при раке прямой кишки.
Распространенность раковой инвазии в дистальном направлении изучалась целенаправленными и тщательными морфологическими исследованиями. R.Willis приводит концепцию «опухолевого поля», в соответствии с которой новообразование развивается мультицентрически с формированием затем единого опухолевого узла. В.Ю.Клур с соавт. проводил серийные гистологические срезы не только в дистальном направлении, но и радиарно. Они установили, что контуры «опухолевого поля» имеют эксцентрическое распространение от основного узла с внутристеночной инвазией, которая в дистальном направлении составляет не менее 3,5-4,0 см при экзофитных опухолях, а при эндофитном росте увеличивается еще на 1,0-1,5 см. Г.И. Воробьев с соавт. исследовал 71 препарат прямой кишки, удаленный при брюшно-промежностной экстирпации. Они установили, что глубина опухолевой инвазии прогрессивно уменьшается в направлении от центра к периферии опухоли. Дистальный внутристеночный рост по подслизистому слою был зарегистрирован лишь в 2,2 % случаев и не превышал 15 мм. Глубина инвазии колоректального рака изучалась также с помощью компьютерного исследования, эндоректоэхографии. В результате была установлена незначительная по протяженности от опухолевого узла внутрикишечная инвазия опухолевого процесса в дистальном направлении. Практически это было претворено в жизнь, и на смену «правила 5 см» пришло «правило 2 см», т. е. достаточно отступить от нижнего края опухоли 2 см с тем, чтобы не нарушить основной онкологический принцип оперирования.
Распространенность опухолевой инвазии в проксимальном направлении в меньшей мере привлекала внимание специалистов. При пересечении кишки выше опухоли не возникает необходимости в строгой экономичности сохранения кишки, примыкающей к опухоли, так как всегда имеется достаточная часть остающегося участка левого фланга ободочной кишки. Вместе с тем наши специальные исследования с анализом длины сигмовидной кишки по дооперационным ирригограммам и размера резецированной части ее после передней резекции ПК показали несомненную важность максимально возможного сохранения для анастомоза дистальной части сигмовидной кишки. К подобному заключению нас подвело изучение функциональных результатов сфинктеросохраняющих резекций ПК. Все это побудило специально изучить распространенность ракового поля в проксимальном направлении от верхнего края видимой опухоли. Результаты таких исследований были нужны для определения минимального расстояния, которое необходимо отступать от верхнего края раковой опухоли при пересечении кишки для соблюдения онкологических принципов оперирования.
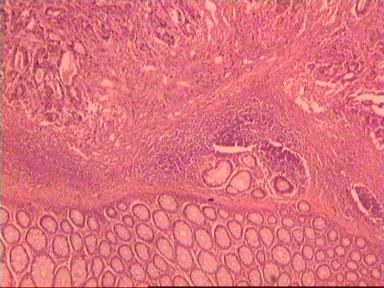
После фиксации препарата в проксимальном направлении от видимого верхнего края опухоли последовательно проводились пересечения кишечной стенки с интервалом 5мм (рис. 1).
Результаты исследования. Представляем наблюдение, характеризующее отсутствие опухолевой инвазии по кишечной стенке.
Мужчина 54 года, рак анального канала и ПК, выполнена брюшнопромежностная экстирпация ПК. Гистологическое исследование 31261−31272.
Макропрепарат: блюдцеобразно возвышающееся над поверхностью кишки новообразование диаметром 6 см, прорастает все стенки кишки. От края опухоли в проксимальном направлении макроскопически определяется инфильтрация стенки на протяжении 3,5 см.
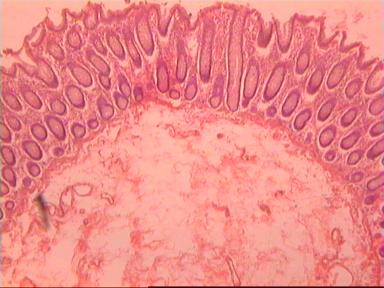
Микроскопическое исследование: высокодифференцированная слизеобразующая аденокарцинома ПК, прорастание всей толщи стенки кишки, врастание опухоли в жировую ткань. В опухоли очаги некроза, выраженная мононуклеарная реакция. От проксимального края видимой инвазии уже в 1 мм внутристеночного роста опухоли нет. (Рис. 2). Метастазов аденокарциномы в лимфатических узлах и жировой ткани не выявлено.
Рис. 2. Микропрепарат слизеобразующей аденокарциномы ПК
Такие данные были получены и при аденокарциноме, и при плоскоклеточном раке ПК. Приведем наблюдение, свидетельствующее о распространении опухолевого роста по кишке в проксимальном направлении. Мужчина 73 года, рак ПК, выполнена передняя резекция ПК. Гистологическое исследование № 869−870; 871−882. Макропрепарат: опухоль 5 см с кратером, циркулярно охватывающая просвет кишки, прорастание всех слоев кишки и прилежащей жировой ткани, участки абсцедирования.
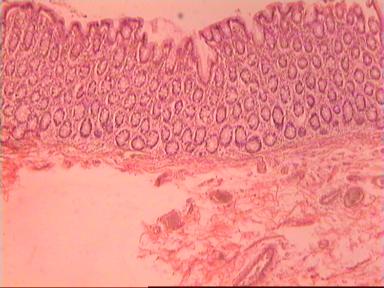
Микроскопическое исследование: аденокарцинома разной степени дифференцировки. В 5 мм вне видимой опухоли − аденокарцинома в подслизистом, мышечных слоях, в клетчатке, с абсцедированием (рис 3). На срезах через 10 мм от видимого края новообразования опухолевого роста нет.
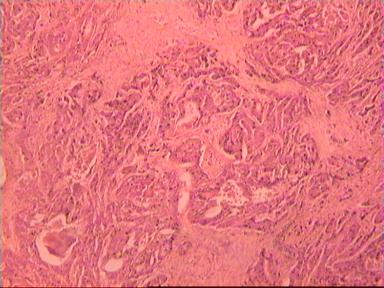 |  |
| А | Б |
Рис. 3. Микропрепарат аденокарциномы ПК разной степени дифференцировки
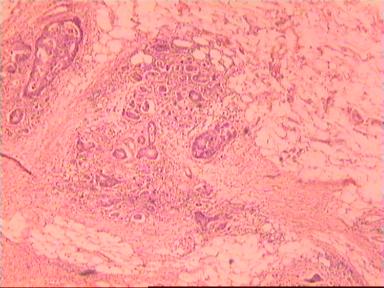
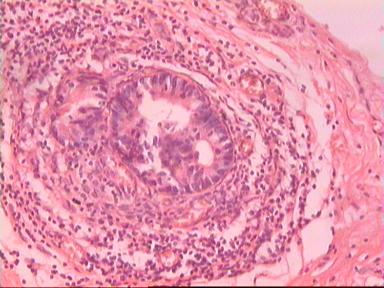
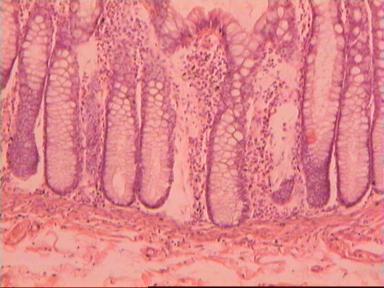
Приведем еще одно наблюдение, свидетельствующее о несомненном распространении опухолевого роста по кишке в проксимальном направлении. Женщина 73 года, рак ПК, выполнена резекция ПК по Гартману. Макропрепарат: экзофитная опухоль 5 х 5 см, прорастание всех слоев кишки, регионарные лимфоузлы не определяются.
 |  |  |
| А | Б | В |
Рис. 4. Микропрепарат аденокарциномы ПК разной степени дифференцировки
Рак прямой кишки. Инвазия опухоли. Обсуждение результатов исследования.
Данные исследования убедительно свидетельствуют, что раковая инвазия в проксимальном направлении от верхнего видимого края раковой опухоли ПК не имеет тенденции к значительному распространению, а в основном ограничена контурами макроскопического «ракового узла» или инвазией по кишечной стенке не более чем на 5мм от него. Лишь в 23,5 % случаев было установлено распространение ракового поля в проксимальном направлении, причем максимально зарегистрированная инвазия была в 20мм от видимого края опухоли ПК.
Вопреки ожиданиям не выявилось повышенной тенденции к внутристеночному росту при низкодифференцированной аденокарциноме, слизистых и плоскоклеточных формах рака ПК. Следовательно, отступление от верхнего края опухоли на 4−5 см в проксимальном направлении с онкологических позиций вполне оправдано и нет необходимости удалять здоровую и функционально полноценную часть кишки. Однако нужно учитывать, что уровень пересечения кишки выше опухоли во многом определяется высотой перевязки основного кровеносного сосуда, которым для этой зоны является нижняя брыжеечная артерия, особенностями кровоснабжения конкретного участка кишки и вовлеченностью в онкопроцесс лимфатического аппарата. Намечая линию пересечения сигмовидной или нисходящей части ободочной кишки, нужно учитывать эти обстоятельства и по возможности бережно, экономно относиться к удалению этого отдела толстой кишки, помня, что инвазия опухоли по стенке кишки незначительна.
Таким образом, внутрикишечная инвазия злокачественного роста в проксимальном направлении от видимого края опухоли ПК наблюдается в 23,5 % случаев и не превышает по протяженности 20 мм. В остальных случаях «раковое поле» ограничивается контурами основного видимого новообразования или распространяется не более чем на 5 мм от него.
Уровень пересечения кишки на 4−5 см выше проксимального края видимой раковой опухоли ПК онкологически оправдан, если учесть распространение «ракового поля» по кишечной стенке. Однако объем операции, конечно, зависит от особенностей кровоснабжения конкретного участка кишки, вовлеченностью в онкопроцесс лимфатических узлов и некоторых других факторов.
Результаты тотальной мезоректумэктомии с применением водоструйной диссекции при раке прямой кишки: взгляд хирурга и патоморфолога
Сидоров Д.В., Франк Г.А., Майновская О.А., Ложкин М.В., Гришин Н.А., Петров Л.О., Троицкий А.А.
Московский научно-исследовательский онкологический институт им. П.А. Герцена, Москва, Россия
В работе приведен собственный, первый в России опыт применения водоструйного диссектора ERBEJET2 ® в ходе выполнения оперативных вмешательств по поводу рака прямой кишки.
Методика водоструйной диссекции на этапе мобилизации препарата применена нами у 5 больных раком прямой кишки. Средний возраст больных составил 58,3±14,2 лет (47-78). В исследованной группе было 2 мужчин и 3 женщины. У всех больных оперативные вмешательства выполняли по поводу аденогенного рака прямой кишки, морфологически верифицированного на предоперационном этапе. Удаленные препараты исследованы морфологически. Для оценки качества хирургического лечения были использованы критерии, разработанные в исследованиях Ph. Quirke. При микроскопическом исследовании циркулярного края резекции, помимо определения хирургического клиренса, оценивали выраженность и глубину повреждения ткани мезоректума. Для сравнения были выбраны две контрольные группы по 5 больных, у которых мобилизацию прямой кишки производили с применением монополярного коагулятора и гармонического скальпеля. Исследованные группы были сопоставимы по гендерному составу, возрасту, локализации и распространенности опухоли. Все оперативные вмешательства выполняла одна бригада хирургов.
Средняя продолжительность операции составила 143±39,1 мин. (от 105 до 190). Объем кровопотери оценен как минимальный во всех 5 наблюдениях. Интраоперационных осложнений не зафиксировано. Течение послеоперационного периода гладкое у всех больных. Дизурические нарушения отсутствовали. Средняя продолжительность послеоперационного пребывания пациентов в стационаре – 9 дней (7-11).
При морфологическом исследовании качество мезоректумэктомии было оценено как хорошее (Grade 3) у всех 5 пациентов. Среднее количество исследованных лимфоузлов составило 24,2±6,4. Метастатическое поражение лимфатических узлов мезоректальной клетчатки выявлено у трех больных. В двух контрольных группах качество мезоректумэктомии также было оценено как хорошее (Grade 3) у всех 10 пациентов. В группе больных, у которых мобилизацию прямой кишки выполняли с применением водоструйной диссекции, повреждения тканей (фасции и клетчатки) практически не отмечалось. Наибольшее повреждение ткани (в виде термического воздействия, вплоть до очагов коагуляционного некроза) по латеральному краю резекции отмечали при использовании монополярного коагулятора. Глубина термического повреждения ткани по латеральному краю в этой группе составила от 1,7 до 3,0 мм. Латеральное повреждение тканей при мобилизации прямой кишки при помощи гармонического скальпеля было менее выражено, чем при использовании монополярного коагулятора. Ткани удаленного препарата практически не имели признаков термического воздействия, и изменения проявлялись преимущественно в деформации тканевых структур. Максимальная глубина повреждения ткани по латеральному краю резекции в данной группе составляла от 1,0 до 1,5 мм.
Водоструйные диссекторы могут занять свое место в списке оборудования, используемого при выполнении оперативных вмешательств по поводу рака прямой кишки и внести свой вклад в улучшение онкологических и функциональных результатов хирургического лечения данной группы больных.
Ключевые слова: рак прямой кишки, тотальная мезоректумэктомия, водоструйная диссекция.
Хирургический метод остается основным в лечении больных раком прямой кишки (РПК). Радикально выполненное оперативное вмешательство позволяет рассчитывать как на достижение локального контроля, так и на хорошие онкологические результаты данной категории больных в целом. Пионерская работа, посвященная технике и отдаленным результатам тотальной мезоректумэктомии (ТМЭ), опубликованная R.J. Heald в 1986 г. [7], положила начало новой эпохе в онкопроктологии. До внедрения в практику рутинного выполнения ТМЭ частота развития местных рецидивов после радикальных операций по поводу РПК, по данным разных авторов, достигала 20-38% [6, 16]. В настоящее время ТМЭ является общепризнанным «золотым стандартом» хирургического лечения рака прямой кишки и позволяет достичь 5-летнего локального контроля у 90-97% больных [1, 10, 12].
Методика ТМЭ подразумевает мобилизацию прямой кишки острым путем под контролем зрения в пределах мезоректальной фасции, с сохранением элементов вегетативной нервной системы таза. Для выполнения такой мобилизации хирурги во всем мире традиционно используют ножницы, коагулятор, в последние годы – гармонический скальпель.
Несмотря на публикации, посвященные возможностям применения водоструйной диссекции на этапе ТМЭ при выполнении внутрибрюшных резекций по поводу РПК [9, 22], данная методика к настоящему моменту не получила широкого распространения в онкопроктологии. Так, в доступной отечественной литературе упоминания об использовании водоструйного диссектора в хирургии РПК отсутствуют, а общее число таких публикаций в зарубежной печати не превышает десятка.
В работе мы приводим собственный, первый в России опыт применения водоструйного диссектора ERBEJET2 ® в ходе выполнения оперативных вмешательств по поводу РПК.
Материалы и методы
Методика водоструйной диссекции на этапе мобилизации препарата применена нами у 5 больных РПК. Средний возраст больных составил 58,3±14,2 лет (47-78). В исследованной группе было 2 мужчин и 3 женщины. У всех больных оперативные вмешательства выполняли по поводу аденогенного РПК, морфологически верифицированного на предоперационном этапе. Объем предоперационного обследования, помимо клинических и лабораторных методов, включал УЗИ (в т.ч. – трансректальное и трансвагинальное) и МРТ органов малого таза. Опухоли локализовались в среднеампулярном (у 3 пациентов) и нижнеампулярном (2 больных) отделах прямой кишки. Расстояние от нижнего полюса опухоли до края ануса варьировало от 4 до 9 см. Латеральное распространение опухоли по результатам предоперационного обследования расценено как Т2 (инвазия мышечной оболочки стенки кишки без выхода в мезоректальную клетчатку) у трех больных, T3 (выход опухоли за пределы стенки кишки) – у двух пациентов. Данных за поражение лимфатических узлов мезоректальной клетчатки и других регионарных зон не было получено ни у одного пациента. Противопоказаниями к проведению предоперационной химиолучевой терапии у больных с опухолевой инвазией мезоректальной клетчатки в одном наблюдении были эпизоды активных кровотечений из опухоли, во втором – наличие синхронных билобарных метастатических очагов в печени.
Использование водоструйного диссектора начинали на этапе мобилизации ректосигмоидного отдела. Строго под контролем зрения мобилизовали заднюю и боковые стенки прямой кишки, при этом выделяли и аккуратно отделяли правый и левый гипогастральные нервы от мезоректума. Благодаря водоструйной диссекции в корректном слое («holy plane») внутритазовая фасция оставалась интактной, покрывая пресакральные сосуды ниже промонториума, внутренние подвздошные сосуды и грушевидные мышцы таза. Возникающее в ходе диссекции капиллярное кровотечение, как правило, не требовало остановки коагуляцией и купировалось самостоятельно. Диссекция продолжалась до тазового дна. Пересечение более плотных соединительнотканных структур производили гармоническим скальпелем или коагулятором.
Далее производили водоструйную диссекцию (при необходимости – с дополнительной обработкой гармоническим скальпелем) в области боковых связок прямой кишки. В большинстве случаев дистальные ветви средних прямокишечных артерий, проходящие в «боковых связках» прямой кишки от внутритазовой фасции к мезоректуму, имеют незначительный диаметр и легко поддаются коагуляции.
После пересечения «боковых связок» продолжали мобилизацию прямой кишки по задней и боковым поверхностям до уровня париетальной тазовой фасции и фасции Вальдейера, идущей от леваторов и покрывающей дистальную часть прямой кишки и аноректальный переход. Пересечение прямой кишки производили при помощи аппарата Countur. После этого приступали к формированию аппаратного колоректального или колоанального анастомоза с формированием превентивной трансверзостомы. Для формирования анастомозов использовали циркулярные сшивающие аппараты.
Удаленные препараты подвергали морфологическому исследованию. Макроскопическое исследование препарата включало оценку сохранности собственной фасции прямой кишки, степени выраженности клетчатки по передней, задней и боковым поверхностям кишки. Для оценки качества хирургического лечения были использованы критерии, разработанные в исследованиях Ph. Quirke [17]. Кроме этого, при микроскопическом исследовании циркулярного края резекции, помимо определения хирургического клиренса, оценивали выраженность и глубину повреждения ткани мезоректума. Для сравнения были выбраны две контрольные группы по 5 больных, у которых мобилизацию прямой кишки производили с применением монополярного коагулятора и гармонического скальпеля. Исследованные группы были сопоставимы по гендерному составу, возрасту, локализации и распространенности опухоли. Предоперационную лучевую терапию не проводили ни одному из 15 пациентов. Все оперативные вмешательства выполняла одна бригада хирургов.
Всем больным выполнены нервосберегающие низкие передние резекции прямой кишки с парааортальной лимфаденэктомией. Одной пациентке дополнительно произведена билатеральная обтураторная лимфаденэктомия. Средняя продолжительность операции составила 143±39,1 мин. (от 105 до 190). Объем кровопотери оценен как минимальный у всех 5 больных. Интраоперационных осложнений не зафиксировано. Течение послеоперационного периода гладкое у всех больных. Дизурических нарушений не было. Самостоятельное мочеиспускание восстановилось на 1-е сутки (после удаления мочевого катетера) у всех 5 пациентов. Средняя продолжительность послеоперационного пребывания пациентов в стационаре – 9 дней (7-11).
При морфологическом исследовании качество мезоректумэктомии было оценено как хорошее (Grade 3) у всех 5 пациентов. Инвазия опухоли в мезоректальную клетчатку рТ3 выявлена у трех больных; опухоль в пределах стенки кишки рT2 – у двух пациентов (у одного больного имела место некоторая недооценка распространенности опухоли по данным предоперационного обследования). Статус CRM расценен как негативный в 4 наблюдениях. В одном случае выявлен опухолевый депозит в мезоректальной клетчатке на расстоянии менее 1 мм от циркулярного края резекции (CRM+). Среднее количество исследованных лимфатических узлов составило 24,2±6,4. Метастатическое поражение лимфатических узлов мезоректальной клетчатки выявлено у трех больных.
В двух контрольных группах качество мезоректумэктомии также было оценено как хорошее (Grade3) у всех 10 пациентов. У двух зафиксирован положительный статус циркулярного края резекции (опухолевый депозит и метастатический лимфатический узел на расстоянии менее 1 мм от CRM).
При исследовании глубины повреждения тканей по латеральному краю удаленного препарата получены следующие данные.
В группе больных, у которых мобилизацию прямой кишки выполняли с применением водоструйной диссекции, повреждения тканей (фасции и клетчатки) практически не отмечалось (рис. 1, 2).
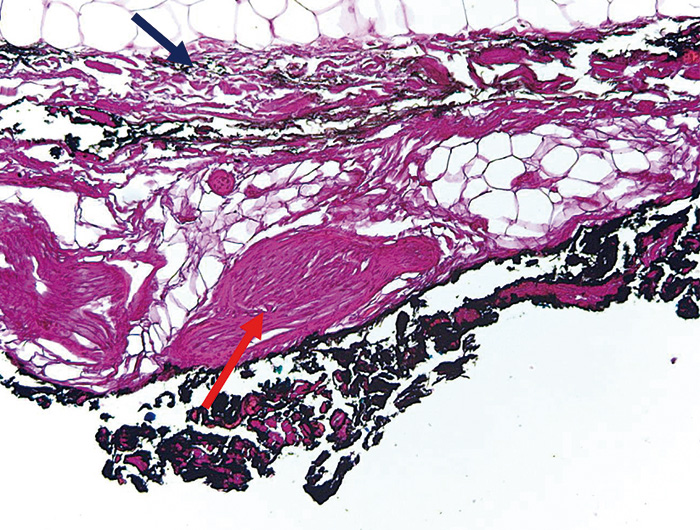
Рис. 1. Макропрепарат. На поверхности мезоректума (вид сзади) при его мобилизации с использованием водоструйного диссектора определяется небольшое разволокнение собственной фасции кишки без ее повреждения.
Рис. 2. Микропрепарат. Мобилизация прямой кишки с использованием водоструйного диссектора. Небольшое разволокнение собственной фасции (окрашена черной краской) без ее деформации (синяя стрелка) и полное сохранение субфасциальных структур – нервных стволов (красные стрелки). Окраска гематоксилином и эозином. Увеличение ×100.
Наибольшее повреждение ткани (в виде термического воздействия, вплоть до очагов коагуляционного некроза) по латеральному краю резекции отмечали при использовании монополярного коагулятора. Причем в большей степени деформации подвергались мезоректальная фасция, элементы боковых связок и резецированные экстрафасциальные структуры (сосуды и нервы). Глубина термического повреждения ткани по латеральному краю в группе больных, оперированных с применением монополярного коагулятора, составила от 1,7 до 3,0 мм (рис. 3, 4).
Рис. 3. Макропрепарат. Поверхность мезоректума (вид сзади) при его мобилизации с использованием монополярного коагулятора: определяются крупные участки термовоздействия (стрелки).
Рис. 4. Микропрепарат. Мобилизация прямой кишки с использованием монополярного коагулятора: широкая зона термического воздействия по латеральному краю резекции (окрашен черной краской) с выраженной деформацией фасции и экстрафасциальных структур – нервных стволов (стрелки). Окраска гематоксилином и эозином. Увеличение ×50.
Латеральное повреждение тканей при мобилизации прямой кишки при помощи гармонического скальпеля менее выражено, чем при использовании монополярного коагулятора. Ткани удаленного препарата практически не имели признаков термического воздействия, и изменения проявлялись преимущественно в деформации тканевых структур. Максимальная глубина повреждения ткани по латеральному краю резекции в данной группе составляла от 1,0 мм до 1,5 мм (рис. 5, 6).
Рис. 5. Макропрепарат. Поверхность мезоректума (вид сзади) при его мобилизации с использованием гармонического скальпеля. Определяются небольшие участки воздействия на уровне боковых связок кишки (стрелка).
Рис. 6. Микропрепарат. Мобилизация прямой кишки с использованием гармонического скальпеля. Умеренно выраженная деформация по латеральному краю резекции (окрашен черной краской) с разволокнением собственной фасции (синяя стрелка) и значительной деформацией экстрафасциальных структур – нервных стволов (красная стрелка). Окраска гематоксилином и эозином. Увеличение ×100.
Принцип водоструйной диссекции долгое время применяли в областях, далеких от медицины (в стекольной промышленности, для обработки металлических изделий и т.п.). Первые упоминания о возможности клинического применения тонкой струи воды под высоким давлением для резекции паренхиматозных органов относятся к началу 90-х годов прошлого века [2]. Несмотря на тот факт, что данная методика является относительно новой, она уже нашла достаточно широкое применение в различных областях хирургии. Основной областью применения водоструйных диссекторов в настоящий момент следует признать хирургическую гепатологию [18, 19, 23]. При этом в мировой литературе имеются многочисленные публикации о применении данной методики в хирургии печени, почек, предстательной железы и в нейрохирургии [3, 22]. В качестве основных преимуществ метода упоминается деликатность разделения тканей, сохранение целостности сосудистых и других трубчатых структур, минимальная травматизация окружающих тканей, отсутствие термического повреждения [18, 23].
Последняя из перечисленных особенностей методики водоструйной диссекции (отсутствие возникновения так называемого «латерального термического повреждения» тканей) обусловливает потенциальные преимущества метода именно при выполнении тотальной мезоректумэктомии. В последние годы многие авторы большое внимание уделяют возможности сохранения элементов вегетативной нервной системы таза (см. выше) при выполнении оперативных вмешательств по поводу РПК [5, 11, 14]. Улучшение функциональных результатов и повышение качества жизни больных при выполнении так называемых «нервосберегающих» передних резекций прямой кишки убедительно показано в большом числе исследований и связано, прежде всего, со снижением частоты урологических расстройств и нарушений сексуальной функции (эректильная дисфункция у мужчин, сухость влагалища и диспареуния у женщин) [4, 13, 20].
С другой стороны, в литературе имеются данные (в т.ч. и экспериментальные) о возможности латерального термического повреждения вегетативных нервов при мобилизации прямой кишки с применением коагулятора и в меньшей степени – гармонического скальпеля [8, 21]. Особенно высок риск травматизации тазовых нервов при работе в «критических точках», в т.ч. у латеральной стенки прямой кишки и на уровне промонториума [15]. В связи с этим существуют даже предложения об отказе от применения в этих зонах каких-либо генераторов и возврате к использованию «острой» диссекции ножницами.
Как показали результаты нашего исследования, глубина латерального повреждения тканей при использовании водоструйного диссектора минимальна, что связано с техническими особенностями метода – диссекция тонкой струей воды комнатной температуры. Аналогичный показатель в группе больных, оперированных с применением монополярного коагулятора и гармонического скальпеля, достигает 1,5 мм и 3,0 мм соответственно. Это обусловливает возможность повреждения элементов вегетативной нервной системы таза даже при точном соблюдении плоскости мобилизации препарата. Такое повреждение, в свою очередь, может существенно ухудшить функциональные результаты операций по поводу РПК за счет денервации соответствующих тазовых структур (мочевого пузыря, предстательной железы, шейки матки и влагалища).
Нам представляется, что применение водоструйного диссектора на этапе мобилизации прямой кишки в зонах максимального риска повреждения нервных структур (уровень промонториума, боковые поверхности мезоректальной клетчатки) позволяет свести к минимуму риск латерального термического повреждения тазовых нервов и избежать связанных с этим осложнений. При этом для мобилизации препарата в зонах, удаленных от описанных нервных структур, вполне возможно применение традиционных методик и генераторов (моно- или биполярная коагуляция, гармонический скальпель). Такое комбинированное применение различных методов разделения тканей позволяет рассчитывать на выполнение действительно «нервосберегающих» резекций прямой кишки без существенного увеличения продолжительности операции.
Таким образом, наш первый опыт применения водоструйного диссектора в ходе тотальной мезоректомэктомии свидетельствует о безопасности и эффективности данной методики. Отсутствие эффекта латерального термического повреждения тканей (в первую очередь – элементов вегетативной нервной системы таза) позволяет использовать данный метод диссекции в «критических точках» мезоректумэктомии без риска повреждения названных структур. Совместное применение водоструйного диссектора и других генераторов позволяет рассчитывать на минимальную травматизацию тазового сплетения и, как результат, лучшие функциональные результаты лечения больных.
Водоструйные диссекторы, с нашей точки зрения, могут занять свое место в длинном списке оборудования, используемого при выполнении оперативных вмешательств по поводу РПК, внести свой вклад в улучшение онкологических и функциональных результатов хирургического лечения данной группы больных.
Согласен Данный веб-сайт содержит информацию для специалистов в области медицины. В соответствии с действующим законодательством доступ к такой информации может быть предоставлен только медицинским и фармацевтическим работникам. Нажимая «Согласен», вы подтверждаете, что являетесь медицинским или фармацевтическим работником и берете на себя ответственность за последствия, вызванные возможным нарушением указанного ограничения. Информация на данном сайте не должна использоваться пациентами для самостоятельной диагностики и лечения и не может быть заменой очной консультации врача.
Сайт использует файлы cookies для более комфортной работы пользователя. Продолжая просмотр страниц сайта, вы соглашаетесь с использованием файлов cookies, а также с обработкой ваших персональных данных в соответствии с Политикой конфиденциальности.