Рак молочной железы
Рак молочной железы — это злокачественный процесс, во время которого новообразования, замещающие ткани органа, подвергаются малигнизации (озлокачествлению). Патологические изменения происходят на клеточном уровне, в железистой ткани и млечных протоках. Если обратиться в диагностический центр на ранней стадии, можно остановить прогресс заболевания.
Симптомы рака
На первой стадии рак молочной железы протекает без выраженных признаков. Если при самостоятельном осмотре, который должна выполнять каждая женщина после менструального цикла, не реже, чем раз в три месяца, обнаружили уплотнения в груди – обязательно следует записаться на консультацию к маммологу.
На второй стадии уже увеличиваются подмышечные лимфоузлы, новообразование увеличивается, озлокачествляются окружающие ткани. Возможно появление метастазов в регионарных лимфоузлах подмышечных впадин. Появляется боль при неосторожных движениях и прикосновениях.
Третья стадия характеризуется поражением лимфатической системы, молочная железа отекает, краснеет, на коже возникают эрозии, переходящие в язвы, сосок втягивается, иногда появляются выделения.
Летальный исход при обращении в первой стадии сравнительно низкий — 9-11%, а на третьей составляет уже 43-60%. В четвертой стадии метастазы распространяются в окружающие органы, прорастают в близлежащие ткани. На этой стадии вылечить удается 1,5% пациентов. Общие симптомы онкологического процесса: уплотнения в молочных железах и слабость, повышение температуры (при определенных формах заболевания), может развивается депрессия. На поздних стадиях развития болезни возникает болевой синдром.
Возможные причины возникновения рака груди
Точные причины злокачественного перерождения новообразований до сих пор не установлены. Однако выявлены факторы, ускоряющие формирование и рост новообразований:
Установлено, что толчком к развитию рака молочных желез могут стать эндокринные нарушения и физиологические параметры — большая или плотная упругая грудь. Из-за тяжести молочной железы нарушается кровоснабжение. Во втором случае прохождение питательных веществ затруднено из-за индивидуального строения.
Запись на консультацию маммолога по телефону:
Диагностика и лечение
Чем раньше обнаружат малигнизацию новообразований, тем больше шансов на выздоровление. Скрининговая (первичная) диагностика выявляет первичные изменения в молочной железе. В комплекс мероприятий входят осмотр у маммолога, хирурга, онколога и консультация эндокринолога. Специалисты центра помогают выявить опухоль на стадии формирования и предотвратить ухудшение состояния. Как уточняющие обследования используются УЗИ молочных желез, маммография, МРТ, КТ, гистологическое обследование и другие виды диагностических процедур.
Лечение назначают каждому пациенту индивидуально. Могут потребоваться: химиотерапия, радио- и лучевая терапия, хирургическое вмешательство, иммунотерапия и использование гормональных препаратов. Иногда различные методы сочетаются.
Опасность самолечения
Если во время самообследования выявлены уплотнения в молочных железах, необходимо сразу же обращаться к врачу. Народные средства возможно использовать только в комплексе с традиционным лечением, предварительно согласовав расширение терапевтической схемы с лечащим врачом. Домашние методы помогают повысить иммунитет и уменьшить болезненную симптоматику, но остановить малигнизацию и восстановить структуру железистой ткани невозможно. К тому же уходит время, метастазы формируются и врастают в окружающие ткани, состояние утяжеляется.
Рак молочных желез опасное заболевание, нет достоверных данных выздоровления без помощи официальной медицины. Отдельные случаи излечения можно считать чудом. Не следует экспериментировать с собственным здоровьем, слишком высока цена — жизнь.
Это не предрак: шесть мифов в диагностике заболеваний молочных желез
В течение жизни многие женщины сталкиваются с заболеваниями молочной железы. Хорошая новость в том, что большинство из них никак не связано с раком и приходится на доброкачественные новообразования. Однако в России многие из этих состояний диагностируются как предраковые заболевания, что приводит к ненужному и, порой, вредному лечению. Мы рассмотрели основные такие диагнозы и международные стандарты их лечения.
Для начала стоит отметить, что изменения груди — это нормально. Большинство из них связаны с естественными процессами — состояние груди может меняться до и во время менструации, беременности или менопаузы. Также на него влияют возраст и принимаемые женщиной гормоны и контрацептивы.
Миф 1: фиброаденомы нужно удалять
Это не так. Фиброаденомы — это небольшие новообразования в груди по форме напоминающие твердые шарики, которые легко перемещаются при нажатии и не вызывают болевых ощущений. Чаще всего фиброаденомы появляются у молодых женщин в возрасте 20-30 лет, риск их появления снижается у женщин в период после менопаузы.
Некоторые фиброаденомы можно прощупать самостоятельно. Но большинство выявляется во время маммографии или ультразвука. Показанием к удалению фиброаденомы считается быстрый рост новообразования. В остальном врачи сходятся во мнении, что фиброаденомы не требуют удаления, если они:
— не влияют на форму груди;
— не мешают самой женщине.
В некоторых случаях удаление подобных новообразований скорее противопоказано — например, у пациенток с множественными, но не растущими фиброаденомами. Поскольку при удалении опухолей могут быть задеты или удалены и здоровые ткани молочной железы.
Миф 2: мастопатия — это предраковое заболевание
Вовсе нет. На самом деле, мастопатия даже не входит в международную классификацию болезней, поскольку является нормальным состоянием груди в определенные жизненные периоды. Появление мастопатии связывают с изменением гормонального уровня в организме, именно поэтому симптомы могут усиливаться и уменьшаться в течение цикла.
Более половины женщин в возрасте 20-50 лет сталкиваются с мастопатией. При этом состоянии характерны изменения текстуры ткани молочной железы — она становится более узловатой, появляются бугорки внутри груди. У многих мастопатия протекает почти бессимптомно, у других же появляются ярко выраженные симптомы, такие как:
— боль или дискомфорт в груди, которые обычно становятся сильнее перед началом менструации и уменьшаются во время критических дней;
— грудь кажется опухшей и тяжелой;
— повышается чувствительность груди;
— боль или дискомфорт в подмышечных впадинах;
— могут образовываться «шишки» в груди, которые увеличиваются перед началом менструации, и уменьшаются после нее;
— также могут появляться зеленые или темно-коричневые выделения из груди.
Мастопатия не повышает риски возникновения рака груди. Согласно международным рекомендациям это состояние также не требует лечения, если симптомы выражены в слабой или средней степени. Для уменьшения дискомфорта могут быть рекомендованы обезболивающие, теплые компрессы, а также более облегающий бюстгальтер.
Лечение мастопатии необходимо только если симптомы мешают женщине и вызывают сильную боль в груди. В таком случае врач может назначить гормональную терапию. Хирургическое вмешательство не рекомендуется.
Миф 3: мастит способствует появлению рака груди
Нет, это не правда. Мастит — это воспаление тканей молочной железы, в большинстве случаев вызванное инфекцией или закупоркой молочных протоков. При мастите грудь может покраснеть и стать теплой на ощупь, появляются болевые ощущения. В некоторых случаях заболевание также вызывает схожие с гриппом симптомы — повышение температуры и появление головных болей. Обычно мастит проявляется только на одной груди.
Наиболее часто это заболевание появляется у женщин, кормящих грудью. По данным ВОЗ в 95% случаев заболевание появляется в первые 12 недель после родов. Инфекция развивается из-за закупорки молочного протока или попадания бактерий внутрь соска при кормлении.
Согласно международным исследованиям, мастит не влияет на повышение риска развития рака молочной железы. При лечении не рекомендуется хирургическое вмешательство. Антибиотики, назначенные лечащим врачом, помогут снять боль и температуру. В случае возникновения абсцесса груди (скопления гноя) требуется удалить его хирургическим путем и затем принимать антибиотики.
Миф 4: все кисты необходимо удалять
Не совсем так. Все зависит от размера кисты. Кисты представляют собой мягкие, легко перемещающиеся комки внутри груди. По форме они обычно круглые или овальные, наполнены жидкостью. Кисты могут появиться в одной или обеих железах. В некоторых случаях также могут возникнуть болевые ощущения в груди перед началом менструации.
Кисты — одно из самых распространенных доброкачественных поражений молочной железы, встречающееся у каждой третьей женщины в возрасте от 35 до 50 лет. Эти новообразования не являются раковыми и не увеличивают шансы развития онкологического заболевания. Однако множественные кисты могут затруднить выявление и диагностику других новообразований в тканях молочной железы.
Небольшие кисты обычно не причиняют неудобств женщине, поэтому они не требует особого лечения или удаления. Многокомпонентные кисты незначительно повышают риск развития рака молочной железы в будущем. Поэтому врач может порекомендовать сделать биопсию ткани груди. Крупные кисты (могут достигать до 2,5-5 см в диаметре) также могут вызывать дискомфорт и болевые ощущения, поскольку оказывают давление на соседние ткани. В таком случае следует обратиться к врачу для удаления жидкости из кисты, это поможет уменьшить неприятные ощущения.
Удаление кист хирургическим путем рекомендуется крайне редко. Хирургическое лечение назначают, если киста содержит жидкость кровяного оттенка или регулярно появляется через определенное время и вызывает неудобства.
Миф 5: травмы груди приводят к раку
Исследований, подтверждающих такую связь, нет.
Посттравматические олеогранулёмы (некроз жировых тканей) молочной железы возникают после операций или лучевой терапии, а также в результате травмирования жировых тканей груди. Это доброкачественное заболевание, при котором в жировых тканях появляются небольшие круглые и твердые новообразования, кожа вокруг которых выглядит покрасневшей и поврежденной. Обычно эти новообразования не вызывают болевых ощущений, но иногда некроз жировых тканей также сопровождается появлением кист, наполненных маслянистой жидкостью. Однако не стоит переживать из-за этого — небольшие кисты не требуют удаления и могут со временем исчезнуть самостоятельно.
Постравматические олеогранулёмы могут появляться у женщин и мужчин любого возраста, но наиболее они распространены среди женщин с избыточным весом и большим размером груди.
Согласно международной практике, удаление посттравматических олеогранулём не требуется, поскольку обычно они не вызывают болевых ощущений и не несут в себе риск развития рака молочной железы. Кроме того, операция может привести к поражению соседних тканей. Однако хирургическое вмешательство рекомендовано в следующих случаях:
— если биопсия ткани не дает достаточно информации, чтобы быть уверенным в диагнозе;
— новообразования не исчезают со временем, но становятся больше;
— если постравматические олеогранулёмы вызывают дискомфорт.
Миф 6: цистаденопапилломы повышают риск рака
Цистаденопапиллома, или внутрипротоковая папиллома — это небольшое доброкачественное образование внутри молочного протока, расположенное ближе к соску. Оно может сопровождаться прозрачными или кровяными выделениями из одной груди и болевыми симптомами. Чаще всего с заболеванием сталкиваются женщины от 35 до 50 лет.
Исследования доказывают, что одиночные папилломы не повышают риск развития рака молочной железы. Однако следует проявить осторожность и сделать биопсию, если:
— у женщины множественные папилломы;
— есть семейная история раковых заболеваний/ предрасположенность;
— папилломы появились в возрасте до 35 лет.
Лечение внутрипротоковых папиллом предполагает хирургическое удаление опухоли.
Может ли мастопатия превратиться в рак груди
Доброкачественные опухоли молочной железы — одни из наиболее распространенных явлений в медицине. Так, более 75% женщин репродуктивного возраста рано или поздно сталкиваются с различными заболеваниями груди. При этом всегда возможно четко определить зло- или доброкачественность патологического процесса.
Самый распространенный недуг молочной железы — мастопатия. Она встречается у порядка 50% женщин в возрасте от 30 до 50 лет. Но может ли эта болезнь перерасти в рак? Как связаны эти заболевания и как их отличить друг от друга? Ответы на эти вопросы вы узнаете в этой статье.
Как связаны мастопатия и рак молочной железы

Дело в том, что фиброзная или кистозная мастопатия рассматривается медиками как риск, толчок к развитию онкологии, а не как предраковое состояние. То есть в некоторых случаях болезнь приводит к раку, но для этого должны быть серьезные предпосылки, например, запущенная форма заболевания.
Сама по себе мастопатия молочной железы — не онкология, это ФКБ (фиброзно-кистозная болезнь), проявляющаяся в виде патологических изменений в железистой ткани груди. На рентгене заболевание рассматривается как череда пятен — светлые (новообразования) и темные (пустоты).
Важно понимать, что женская грудь — гормонозависимая железа. И любые нарушения в работе эндокринной системы быстро сказываются и на ней. А цепочки гормональных процессов, которые приводят к ФКБ, могут быть совершенно разными, поэтому определить, может ли мастопатия привести к раку, порой просто нереально.
Даже факторы, которые могут спровоцировать развитие онкологии и мастопатии, одинаковые:
Как отличить мастопатию от рака молочной железы
Явные отличия онкологии грудной железы и мастопатии симптоматически отличить непросто. Сделать это может исключительно опытный маммолог и лишь по заключению инструментального исследования груди. Ведь как при раке, так и при мастопатии, в груди можно обнаружить новообразования разного размера и степени болезненности. Также при обоих заболеваниях могут наблюдаться различные выделения из сосков. Поэтому чтобы понять, какой именно недуг поразил грудь, необходимо пройти ультразвуковое исследование или маммографию.
Главное отличие мастопатии от рака молочной железы заключаются в том, что боли в груди, выделения и уплотнения появляются временно — перед началом менструального цикла, а после его завершения — исчезают. При онкологии эти проявления будут постоянными. Поэтому при этих симптомах крайне важно быстрее обратиться к маммологу, пройти УЗИ и маммографию. Если рак все же подтвердится, срочно начать лечение. Ведь при ранней терапии шансы на ее успех максимальны.
Многие женщины интересуются, как отличить мастопатию от рака методом самопальпации груди? Увы, даже опытный маммолог не всегда может понять, какие именно уплотнения он выявляет — фиброзно-кистозные или онкологические. Поэтому пациенток направляют на дополнительные исследования — УЗИ и маммографию:
Путь клетки «из греков в варяги». Малигнизация: причины и следствия
Малигнизация — один из самых загадочных процессов. Что же на самом деле направляет клетку на тернистый путь перерождения?
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Недуг, прозванный чумой XXI века. В наши дни рак является одним из самых страшных заболеваний. В 2010 году более семи миллионов людей по всему свету умерли от рака. В Соединенных Штатах каждая третья женщина и каждый второй мужчина рано или поздно заболеют раком. По прогнозам ВОЗ, число случаев заболевания будет продолжать расти от 14 миллионов в 2012 году до 22 миллионов в следующие десятилетия. Пугающие числа, от которых невольно бросает в дрожь. Однако процесс ракового перерождения, или малигнизации, не только страшен, но и интересен, и в этой статье мы разберемся, почему же некоторые «избранные» клетки решают свернуть не туда и как это влияет на самого «изменника».
Конкурс «био/мол/текст»-2019
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2019.

Генеральный спонсор конкурса и партнер номинации «Сколтех» — Центр наук о жизни Сколтеха.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий выступила компания BioVitrum.
Гончие еще играют во дворе, но дичи не уйти,
как ни мчится она уже сейчас по лесам.
Франц Кафка
На «Биомолекуле» опубликовано немало статей о молекулярных основах канцерогенеза. Но каждая из них, как правило, посвящена какой-то одной стороне этого патологического процесса, в то время как среди наших читателей наверняка есть люди, которые хотели бы, прежде чем углубляться в детали, получить общее представление о раковой клетке. Обзорная статья Анны Батуевой удачно заполняет этот пробел и дает общее представления о ключевых молекулярных механизмах злокачественного перерождения. — Ред.
Под малигнизацией понимают приобретение здоровыми клетками черт злокачественности, которые мы подробно рассмотрим ниже. Процесс злокачественного изменения можно уподобить дичи из цитаты Кафки, ведь клетка, однажды встав на этот путь, не сможет вернуться и получить свое клеточное здоровье обратно. Важную роль в понимании основ перерождения клеток и их дальнейшего функционирования сыграла медицина, а следом за ней и молекулярная биология. Но начнем с истоков истории рака.
Часть 1. Биография рака
Первые упоминания о раке встречаются в папирусе Эдвина Смита, датируемом 16 веком до нашей эры [1]. Там же отмечается, что данное заболевание не поддается лечению.
Во времена Гиппократа, около 400 года до нашей эры, появилось специальное обозначение рака — karkinos. Разросшаяся опухоль напомнила Гиппократу краба, окутывающего все вокруг клешнями. Современное название онкологии произошло от греческого слова onkos, которое греки использовали для описания опухолей. Однако врачи того времени не различали доброкачественные и злокачественные новообразования, и karkinos Гиппократа не имеет ничего общего с истинным раком.
Гиппократ выдвинул гуморальную теорию, суть которой состояла в том, что каждый недуг является следствием переизбытка одного из четырех гуморов: крови, слизи, желтой желчи и черной желчи.
Гален, греческий врач, практиковавший в Риме около 160 года нашей эры, довел теорию Гиппократа до совершенства. Он заявил, что рак образуется из-за переизбытка черной желчи. Гален умер в 199 году нашей эры, но его «черная желчь» еще долго будоражила умы онкологов.
Только спустя пять столетий, в 1538 году, Андреас Везалий опроверг теорию Галена, делая вскрытия в Парижском университете. Окончательно похоронил галенову теорию лондонский анатом Мэтью Бейли, который в 1793 году опубликовал учебник «Патологическая анатомия некоторых наиболее важных частей человеческого тела» [2], в котором представил рисунки и описания раковых опухолей, где не было и следа «черной желчи».
Изобретение микроскопа повлекло за собой первые цитологические исследования рака. В 1801 году французский физиолог Франсуа Биша и в 1838 году Иоганн Мюллер определили, что опухоли имеют клеточную структуру. После этого Жан Крювелье высказал гипотезу «канцероматозной дегенерации», основанную на предположении, что клетка проходит несколько этапов, прежде чем окончательно превратиться в раковую. Немецкий хирург Карл Тирш доказал, что раковая опухоль происходит из эпителиальной ткани, а саркома — из соединительной.
Первая половина XX века породила еще одну теорию канцерогенеза, недалеко ушедшую от истины. В 1911 году Пейтон Раус, работая в Рокфеллеровском университете в Нью-Йорке, открыл вирус, способный вызывать опухоли у кур. Ученые по всему свету бросились искать вирусы, ответственные за рак именно у человека, однако ничего не могли найти. В 1974 году в Medical World News вирус рака у человека ставили в один ряд с НЛО, снежным человеком и лохнесским чудовищем. Вирус СВ-40 и вирус папилломы человека, вызывающие рак у людей, были открыты в 1960 и 1983 годах соответственно.
В 1970 году генетик Говард Темин, работавший в лаборатории Макардла в Висконсине и изучавший вирус саркомы Рауса (ВСР, или VSR), представил свою работу на Десятом Международном онкологическом конгрессе. Он открыл у ВСР обратную транскрипцию — синтез ДНК по РНК — и положил начало изучениям ретровирусов. Позднее он отказался от вирусной теории канцерогенеза, а в 1979 году ученые Майкл Бишоп и Харолд Вармус открыли первый протоонкоген — src (сарк), содержащийся в ВСР. Это положило начало новому этапу в истории онкологии, люди наконец-то поняли, как запускается процесс канцерогенеза. Но этого бы не произошло без изучения раковой клетки и ее странной физиологии.
Часть 2. Что заставляет клетку измениться?
В этой главе мы разберем причины злокачественного перерождения клетки. Первым толчком к началу этого изменения является мутация в ДНК.
Но не всякие повреждения ДНК обязательно приведут к появлению раковой клетки, а лишь те, что затронут определенные гены. Наиболее важную роль в канцерогенезе играют три группы генов: протоонкогены, онкогены и гены — супрессоры опухолей.
Протоонкогены
Протоонкогены — это «здоровые» предшественники онкогенов, которые в результате мутации могут вызвать развитие опухоли. Такими причинами являются различные мутации или суперэкспрессия гена. Как правило, протоонкогены кодируют белки, участвующие в процессах жизненного цикла клетки. В результате мутаций появляются сбои в регуляции клеточного деления и дифференцировки.
Основные изменения, происходящие с протоонкогенами:
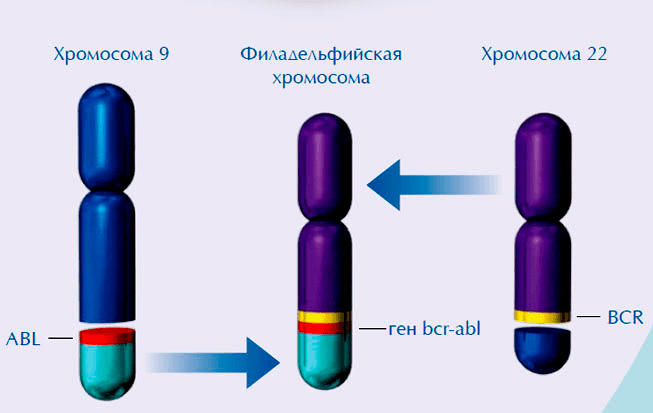
Рисунок 1. Химерный ген BCR-ABL образуется при слиянии участка 9 хромосомы, несущей ген ABL, с участком 22 хромосомы, несущей ген BCR
В некоторых случаях канцерогенез запускается вирусами. Онкогены в геноме вирусов являются ранее захваченными в клетках-хозяевах нормальными генами, которые со временем превратились в злокачественные. Когда такие онкогенные вирусы попадают в клетку, начинается считывание информации с вирусной ДНК или РНК, в цитоплазме накапливаются онкогенные белки и начинается процесс перерождения.
Онкогены
Онкогены — это гены, активность которых стимулирует образование и развитие злокачественной опухоли. Как уже было упомянуто выше, первый вирусный онкоген был открыт в 1979 году.
Биохимические продукты онкогенов
Онкогены кодируют белки с различной структурой и функциями. К основным продуктам деятельности онкогенов относят:
Все вышеперечисленные продукты онкогенов являются сигналами к запуску неконтролируемого клеточного деления. Внешние факторы больше не играют никакой роли в жизни клетки, потому что пролиферацию запускают внутренние сигнальные белки.
Гены и белки — супрессоры
В здоровой клетке существуют защитные механизмы, следящие за процессами и регулирующие клеточный цикл. К таким механизмам относят деятельность белков — супрессоров опухолей: p21, p53, pRb, PTEN и др.
Белок p53 — наиболее изученный белок-супрессор. Он является продуктом гена TP53, мутации которого обнаруживаются в клетках многих опухолей [7]. p53 синтезируется во всех клетках организма, но активируется только при повреждениях ДНК. Этот белок способен остановить клеточный цикл и не допускать дальнейшее деление клетки, пока не произойдет репарация ДНК. При сильных повреждениях он также может запускать процесс апоптоза.
Одной из главных функций p53 является сохранение генетической идентичности всех клеток организма. При неправильной работе этого белка клетка получает возможность делиться даже при поврежденной ДНК, что увеличивает вероятность мутаций и накопления дефектных онкогенов. Важную роль в подавлении p53 играет белок MDM2, который в норме регулирует активность p53. Однако при повышенном синтезе он связывается с p53 и ингибирует его противоопухолевое действие.
Эпигенетические факторы рака
Важными факторами канцерогенеза являются эпигенетические события. Эпигенетика изучает процессы, затрагивающие активность генов, но не изменяющие структуру ДНК. К ним относится изменение метилирования ДНК.
Метилирование — это присоединение метильной группы к нуклеотидам в особых, строго определенных участках генома, называемых CpG-островками. Такое изменение не влияет на структуру молекулы, однако может влиять на экспрессию отдельных генов. В частности, если в участке ДНК много метильных групп, то транскрипция этого участка прекращается.
Особенно активно метилирование проходит в эмбриональный период жизни, а у взрослого человека метилировано около 2% генома. В норме баланс между метилированием и деметилированием строго регулируется и соблюдается, однако в старости начинают преобладать процессы метилирования, что может в итоге привести к канцерогенезу. В процессе онкогенеза происходит гиперметилирование CpG-островков, что приводит к общей геномной нестабильности и накоплению еще большего количества мутаций. В большинстве случаев метилированные участки являются промоторами и влияют на активацию или, наоборот, инактивацию генов, что с виду похоже на действие точечных мутаций.
Однако хотя нарушения в эпигенетической регуляции сопровождают развитие злокачественного перерождения, они, как правило, не являются его первопричиной, а лишь одним из сопутствующих факторов.
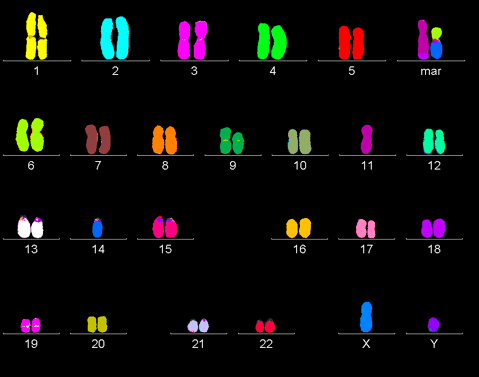
По отдельности каждое из вышеперечисленных нарушений не может спровоцировать раковое перерождение. Все они работают совместно и слаженно. Так, онкогенез запускается, только если одновременно активированы онкогены и инактивированы гены-супрессоры в обеих копиях ДНК. Впервые теорию двойного канцерогенеза высказал Альфред Кнудсон, изучавший ретинобластому: «По всей видимости, — писал он, — в возникновении рака у детей ключевую роль играют два типа генов. Первый, онкогены, действует посредством повышенной, аномальной активности. Второй же класс, антионкогены, в онкогенезе рецессивен: рак происходит лишь тогда, когда обе нормальные копии удалены или изменены» [8]. В процессе жизнедеятельности раковая клетка накапливает все большее количество мутаций, поэтому раковый геном часто очень сильно отличается от генома здоровой клетки (рис. 2).
Рисунок 2. Раковый геном. В процессе жизнедеятельности раковая клетка накапливает огромное количество мутаций и нередко характиризуется полиплоидностью.
Часть 3. Физиологические последствия малигнизации
Основное последствие малигнизации — клеточное бессмертие. Оно может поддерживаться несколькими способами: активацией фермента теломеразы, блокировкой регуляторов митохондриального пути апоптоза и в некоторых случаях активацией механизма ALT (alternative lengthening of telomeres, альтернативного удлинения теломер [14]).
Обратная сторона «вечной молодости»
Впервые клеточное бессмертие раковых клеток было продемонстрировано в 1951 году на клеточной линии HeLa, взятой у Генриетты Лакс, вскоре скончавшейся от рака шейки матки (рис. 3) [9].
Рисунок 3. Клеточная линия HeLa — «бессмертная» линия раковых клеток. С 50-х годов прошлого столетия используется для изучения поведения раковых клеток и выявления новых противораковых препаратов.
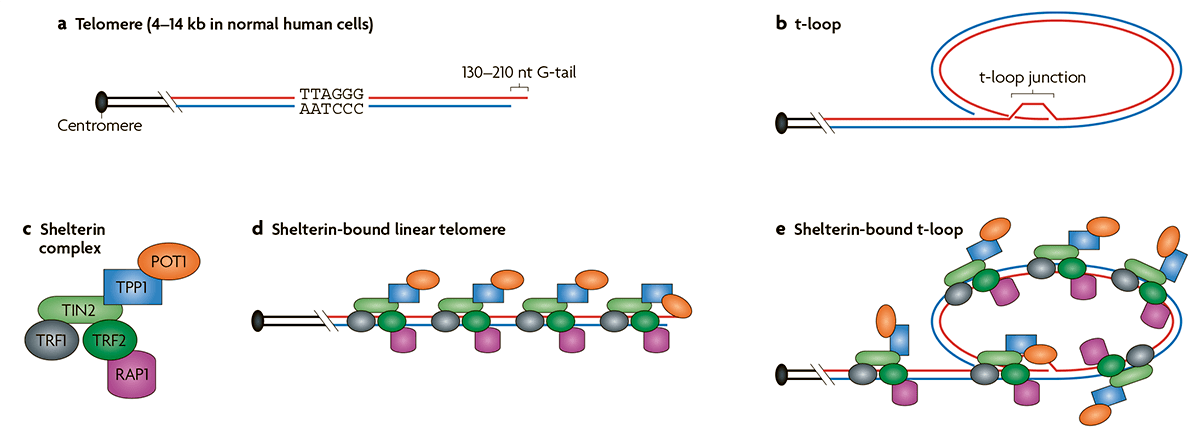
Как правило, малигнизация сопровождается активацией фермента теломеразы. На концах хромосом находятся короткие повторяющиеся участки ДНК, названные теломерами [10]. После каждого деления теломеры укорачиваются, что в итоге приводит к их полному исчезновению и невозможности продолжать деление. Количество возможных делений для клетки названо пределом Хейфлика. Действие теломеразы заключается в восстановлении теломер и превращении клетки в фактически бессмертную, позволяя ей делиться бесконечно долго. Существуют нормальные клетки, в которых также экспрессируется теломераза. Это клетки, которым надо часто делиться: половые, стволовые и клетки эпителия кишечника. Однако теломераза активна в подавляющем большинстве раковых клеток, что играет важную роль в их жизненном цикле.
С другой стороны, в некоторых злокачественных клетках, наравне с активной теломеразой, существует так называемое альтернативное удлинение теломер, или сокращенно ALT [11]. При ALT происходит гомологичная рекомбинация концевых участков хромосом (рис. 4). В норме рекомбинация происходит в процессе мейоза, однако раковые клетки научились достраивать теломеры, используя теломеры другой хромосомы как матрицу [12].
Рисунок 4. Принцип действия ALT, основанный на гомологичном достраивании концов теломер. Такой механизм «бессмертия» является основным для ряда опухолей.
Важно отметить, что раковое бессмертие контролируется не только теломерами, но и ингибированием путей апоптоза, главным из которых является митохондриальный путь. В норме, из митохондрий в цитоплазму выходят митохондриальные белки и образуют апоптотический комплекс — апоптосому, которая и запускает апоптоз. При неправильной работе регуляторных белков, а к ним относятся белки семейства BCL-2, нарушается выход апоптотических белков, что приводит к сбою в процессе апоптоза. В раковых клетках обнаружены нарушения в работе белков BAX и BAK, а также экспрессия ингибиторов клеточной смерти.
Часть 4. Заключение
Ежедневно в нашем организме появляются клетки, вступившие на путь ракового перерождения. Но далеко не все из них дойдут до конца и образуют злокачественную опухоль. С другой стороны, интересно клеточное поведение в процессе малигнизации, когда клетка способна «выключать» отдельные гены, мешающие ее перерождению. Современные исследования в области молекулярной онкологии и раковой геномики дают повод надеяться на окончательное понимание основ малигнизации и физиологии злокачественных клеток. Также в последнее время проводятся разработки новых противораковых препаратов, направленных на исправление дефектных сторон «больных» клеток. Возможно, изучение именно особенностей раковой клетки приведет к созданию лекарства, способного снизить страшные прогнозы Всемирной организации здравоохранения.